Jesteśmy grupą naukowców i inżynierów, wspieranych przez polskich aniołów biznesu. Połączyła nas wspólna pasja do optyki fizycznej, elektroniki, informatyki i inżynierii biomedycznej. Z tej pasji i w oparciu o wieloletnie doświadczenie naukowo-badawcze, tworzymy światowej klasy urządzenia do obrazowania oka, aby wspierać diagnostykę chorób oczu i terapie genowe, przeciwdziałające utracie wzroku.
Publikacji
Patenty
Lat doświadczeń
Współpracujących ośrodków naukowych
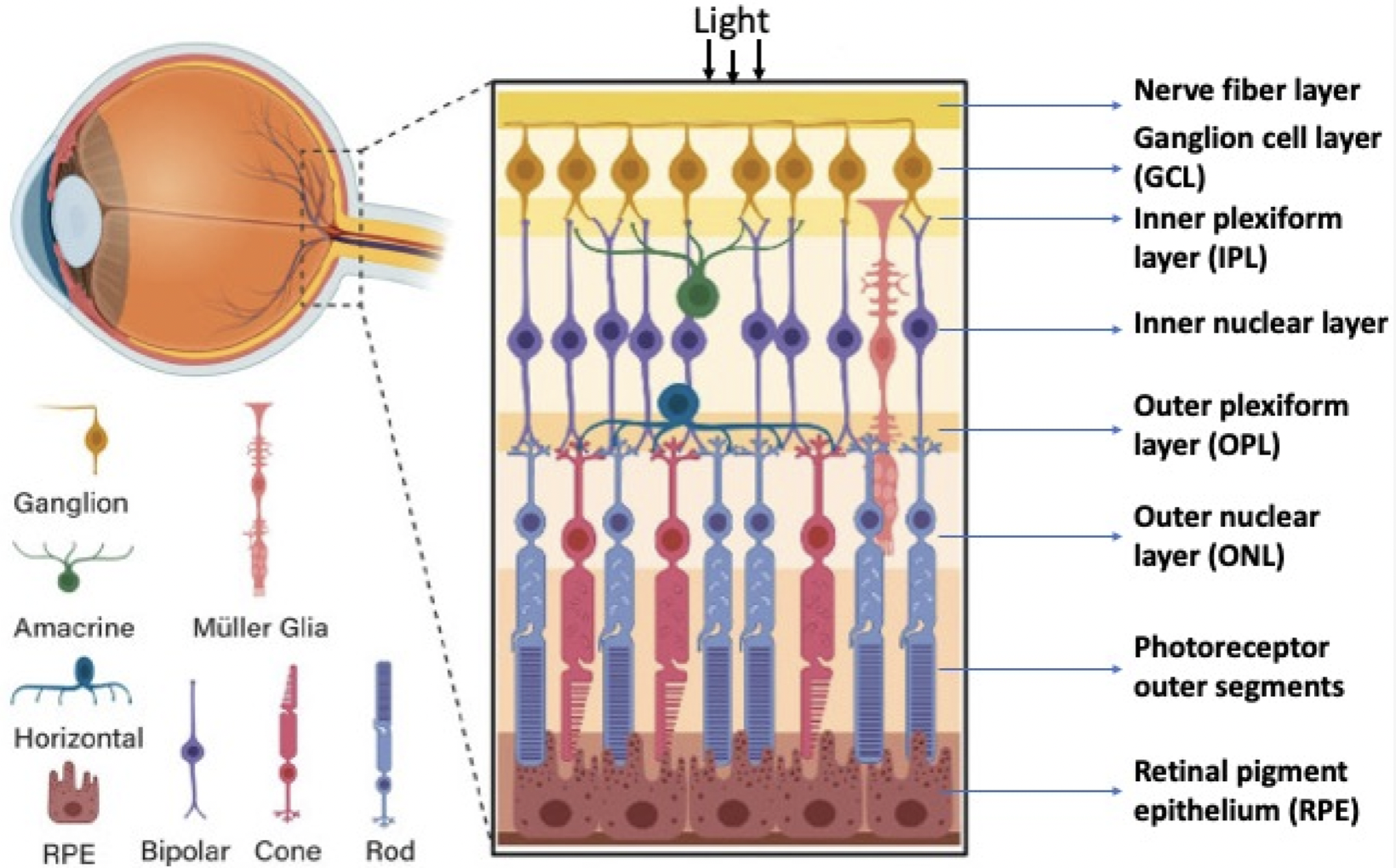
Siatkówka ma ściśle określoną strukturę warstwową, która działa jak popularne obecnie sztuczne sieci neuronowe. W dolnej części siatkówki znajdują się fotoreceptory (photoreceptors), które rejestrują padające światło. Informacja z fotoreceptorów jest przekazywana do płytszych warstw (komórki GCL) za pomocą komórek zlokalizowanych w warstwie INL. Włókna nerwowe (warstwa NFL) przekazują sygnał dalej do mózgu, gdzie są tworzone obrazy.
Proces ten odbywa się bardzo szybko. Z codziennego doświadczenia wiemy, że dzięki szybkiemu działaniu narządu wzroku jesteśmy w stanie realizować złożone działania i szybko reagować na zagrożenia.
Prawidłowe działanie narządu wzroku (jak każdego innego organu) wymaga też składników odżywczych, dostarczanych przez naczynia krwionośne, znajdujące się w głębokich (choroid) i płytkich warstwach siatkówki.
Jednak, z wiekiem i na skutek różnych schorzeń działanie fotoreceptorów, komórek zwojowych i przepływów krwi ulega uszkodzeniu, co w skrajnych przypadkach prowadzi do zaburzenia lub nawet całkowitej utraty wzroku.
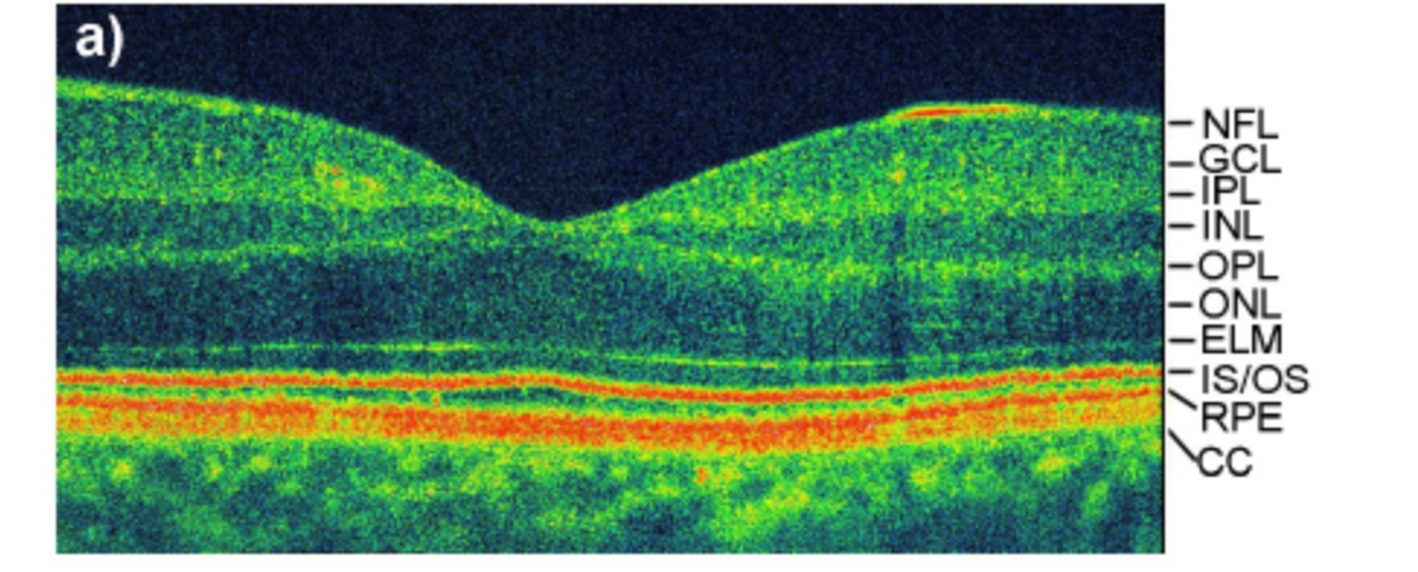
Aby móc analizować strukturę i funkcję oka gabinety okulistyczne są wyposażone w różnego rodzaju instrumenty obrazujące. Jedną z najpopularniejszych technik obrazowania jest tomografia optyczna OCT (optical coherence tomography).
Chociaż instrumenty OCT są tak stabilne, że pracują nawet na stacji kosmicznej, to jednak technologia OCT posiada podstawowe ograniczenia fizyczne, które nie pozwalają na jednoczesne wysokorozdzielcze obrazowanie wszystkich warstw siatkówki. W praktyce zwiększanie rozdzielczości poprzecznej (XY) zmniejsza zakres obrazowania (Z). Dodatkowo, rozdzielczość XY jest ograniczona przez naturalne aberracje (niedoskonałości) oka. Jednym z rozwiązań tego problemu jest zastosowanie optyki adaptacyjnej (adaptive optics). Kilka laboratoriów optycznych skonstruowało instrumenty AO-OCT. Jednak są one bardzo skomplikowane, niestabilne i wymagają eksperckiej wiedzy, przez co AO-OCT nie udało się jeszcze wdrożyć w gabinetach okulistycznych.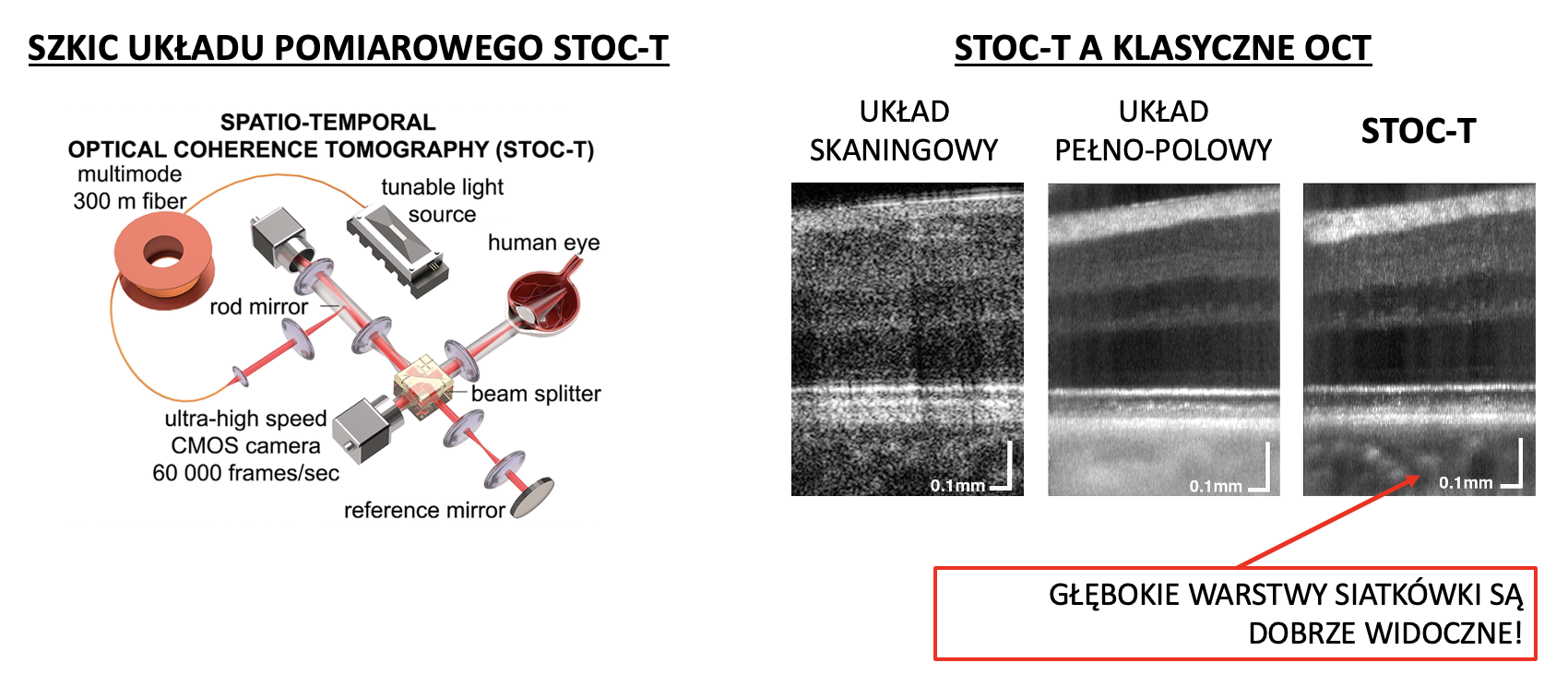
Konwencjonalna skanująca technika OCT (ang. Optical Coherence Tomography) łączy bramkowanie czasowe z konfokalnym, umożliwiając szybkie, wysokorozdzielcze obrazowanie przekrojowe ludzkiej siatkówki. Klasyczna OCT nie zapewnia jednak wysokiej rozdzielczości obrazów głębokich warstw siatkówki ze względu na aberracje oka i fundamentalny kompromis między głębokością obrazowania a rozdzielczością poprzeczną.
Ten kompromis jest redukowany przez metodę pełnopolowej OCT (ang. Full-field OCT, FF-OCT), która wykorzystuje dwuwymiarową kamerę zamiast jednoelementowej fotodiody. Jednak próba zwiększenia szybkości obrazowania FF-OCT poprzez detekcję w dziedzinie Fouriera (FD) spowodowała kolejne poważne ograniczenie. Mianowicie, spójność przestrzenna lasera generuje koherentne artefakty, co zmniejsza rozdzielczość przestrzenną i, jak pokazano powyżej, wyklucza wizualizację głębokich warstw siatkówki.
Aby rozwiązać ten problem, opracowaliśmy nowy sposób kontroli fazy optycznej nazwany STOC (Spatio-Temporal Optical Coherence). Zastosowanie STOC do pełnopolowej optycznej koherentnej tomografii Fouriera (FD-FF-OCT) nazwaliśmy tomografią STOC (STOC-T) lub obrazowaniem STOC. Nasza nowa metodau możliwiła wysokorozdzielcze przyżyciowe wizualizowanie ludzkiej skóry, siatkówki i rogówki z niespotykanymi dotąd prędkościami (100 wolumenów na sekundę).

W obrazowaniu STOC rozszerzyliśmy FD-FF-OCT o przestrzenny modulator fazy (ang. Spatial Phase Modulator, SPM). SPM dynamicznie moduluje fazę padającego światła poprzez generowanie zmiennych w czasie modów poprzecznych (ang. Transverse electromagnetic modes, TEMs). Jest to osiągane poprzez zastosowanie aktywnych modulatorów lub długich światłowodów wielomodowych. Powstałe w ten sposób sygnały są przetwarzane i uśredniane w celu uzyskania wolnych od szumów obrazów objętościowych próbki. Modulacja fazy działa tutaj jako dodatkowy mechanizm bramkowania optycznego, który izoluje użytecznych sygnał. W rezultacie otrzymujemy ulepszone obrazy próbki.
Jednakże obrazy en face (projekcje XY) są zniekształcone przez aberracje wywołane przez oko lub próbkę. Zwalczamy je w post-processingu za pomocą obliczeniowej korekcji aberracji (ang. Digital Aberration Correction, DAC). Algorytm DAC przebiega w sposób przedstawiony na rysunku. W szczególności, iteracyjnie (w komputerze) korygujemy fazę widma przestrzennego w celu optymalizacji metryki ostrości/jakości obrazu. Aby uzyskać obrazy siatkówki w szerokim polu widzenia, wykonujemy pomiary w różnych miejscach, a następnie łączymy ze sobą wynikowe wolumeny, aby wyrenderować wysokiej rozdzielczości obrazy siatkówki na różnych głębokościach (wskazanych wcześniej). W szczególności, renderujemy naczyniówkę (choroid), co było niemożliwe w przypadku konwencjonalnego FF-OCT z domeną Fouriera (bez modulacji fazy).
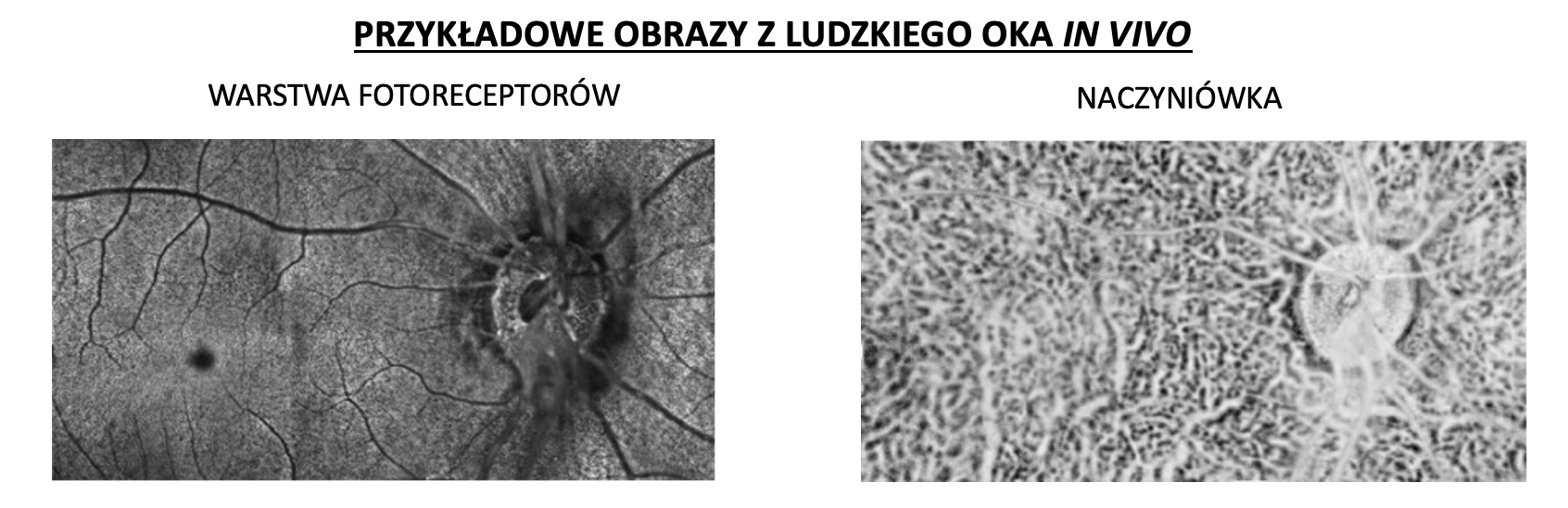
W ramach optoretinografii monitorujemy subtelne zmiany fazy między błoną graniczną (inner and outer photoreceptor junction – IS/OS) a końcówkami zewnętrznego segmentu czopków (ang. cone outer segment tips – COST). Umożliwia nam to śledzenie zmian rozmiarów fotoreceptorów (wzdłuż osi Z), skąd uzyskujemy informacje o działaniu fotoreceptorów w oku pod wpływem pobudzenia światłem. Połączenie takiej analizy dla różnych pozycji XY pozwala nam również klasyfikować białka fotoreceptorowe czopków i pręcików. Badania te wymagają jednak segmentacji obrazów XY aby izolować poszczególne fotoreceptory. Po zidentyfikowaniu tych komórek możliwe staje się diagnozowanie schorzeń wzroku i monitorowanie wdrożonych terapii lekowo-genowych. W tym przypadku monitorujemy fazę, gdyż fotoreceptory wydłużają się o ok 1 nanometr! Taka rozdzielczość jest poniżej rozdzielczości osiowej jakiegokolwiek instrumentu optycznego.
Przykładowe wyniki pokazujące odpowiedzi siatkówki zaadaptowanej do ciemności na pojedynczy impuls światła pokazano na Rys. (b,c). Rysunek (b) przedstawia uśredniony przestrzennie sygnał ORG w funkcji czasu zarejestrowany dla równomiernie rozłożonego bodźca. Natomiast rys. (c) pokazuje maksymalną amplitudę sygnału ORG na obrazowanej części powierzchni siatkówki w odpowiedzi na stymulację wzorem zawierającym literę E.
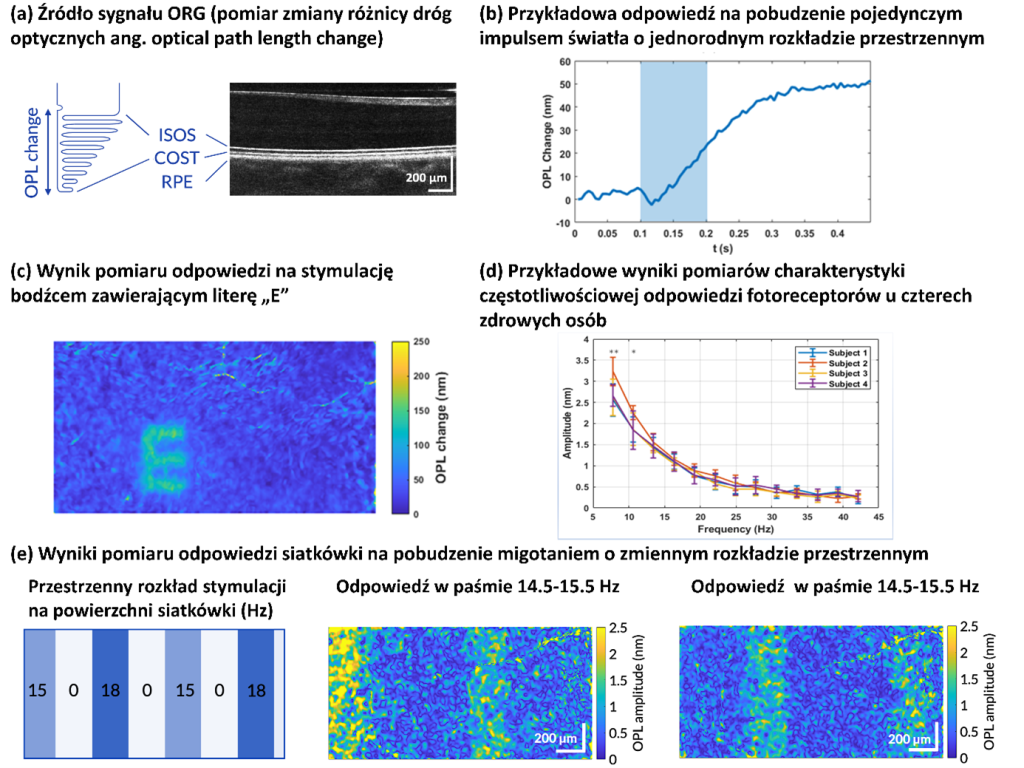
W eksperymentach f-ORG (ang. Flicker ORG), które są główną tematyką naszych prac, do stymulacji siatkówki wykorzystywane jest migoczące światło. Nasza metodologia f-ORG pozwala na pomiar odpowiedzi siatkówki w szerszym zakresie częstotliwości i mapowanie odpowiedzi fotoreceptorów na migoczące światło na powierzchni siatkówki. Przykładowe wyniki zmierzonych charakterystyk częstotliwościowych odpowiedzi u czterech zdrowych osób przedstawiono na rys. (d). Natomiast przykład przestrzennie wykrytej odpowiedzi siatkówki na bodziec projektowany przy użyciu DMD z paskami światła migoczącymi z różnymi częstotliwościami przedstawiono na rys. (e).
Zastosowanie ultra-szybkiej kamery pozwala nam rejestrować wolumeny z wysoką prędkością. Jeden wolumen (512x512x512 pixeli, ok. 130 Mpx) rejestrujemy w czasie krótszym niż 10 ms. Dla porównania wykonanie zdjęcia 2D (48 Mpx) nowoczesnym smartfonem zajmuje ok. 1-2 sekundy (sam czas naświetlania może być krótszy, ale smartfon nie pozwala na tak szybkie powtarzanie zdjęć). Tak szybka rejestracja generuje olbrzymie zbiory danych. W ciągu 1 sekundy uzyskujemy ok. 25 Gb surowych danych, co sprawia, że stajemy przed koniecznością zastosowania zaawansowanych i szybkich algorytmów przetwarzania danych.
Przetwarzanie tak olbrzymich zbiorów danych w krótkim czasie wymaga zastosowania nowych metod obróbki danych opartych o techniki sztucznej inteligencji. W InCellVu wykorzystujemy te metody w trzech aspektach. Po pierwsze, automatyzujemy segmentację warstw siatkówki (wzdłuż osi Z). Po drugie, wykorzystujemy konwolucyjne sztuczne sieci neuronowe do automatycznego wykrywania komórek w obrazach en face (XY). Po trzecie, metody sztucznej inteligencji wykorzystujemy do szybkiego przetwarzania danych z kamery.

Jest fizykiem specjalizującym się w optyce stosowanej, a także fizyce medycznej i eksperymentalnej. Od 2016 r. prof. M. Wojtkowski kieruje Zakładem Fizyki Chemicznej Układów Biologicznych w Instytucie Chemii Fizycznej Polskiej Akademii Nauk, Grupa POB. Jest założycielem i dyrektorem Międzynarodowego Centrum Badań Oka w Warszawie, ICTER (International Center for Transnational Eye Research).
Głównym przedmiotem jego badań jest rozwój nowych technik obrazowania in vivo, tomografii optycznej OCT i interferometrii nisko koherentnej stosowanych w obrazowaniu biomedycznym. Ma znaczący wpływ na rozwój techniki OCT w dziedzinie Fouriera (FD-OCT). Już jako student zademonstrował skuteczność tej metody do obrazowania ludzkiego oka in vivo. Kierował lub kieruje projektami naukowymi o łącznej wartości ponad 50 mln PLN.
Projektuje i rozwija nowe urządzenia biomedyczne oparte na interferometrii światła do nieinwazyjnego, ultraszybkiego obrazowania i analizowania ludzkich tkanek in vivo.
Jego doświadczenie obejmuje rozwój oprogramowania (przetwarzanie sygnałów i obrazów, oraz sterowanie urządzeniami), symulacje numeryczne, planowanie eksperymentów oraz projektowanie i kierowanie złożonymi zadaniami badawczymi. W ramach stażu naukowego w University of California Davis opracował i wdrożył technikę iNIRS do nieinwazyjnego monitorowania funkcji mózgu in vivo.
Magister ekonomii Uniwersytetu Ekonomicznego w Katowicach i Wyższej Szkoły Handlowej z Tuluzy z zakresu Inżynierii finansowej i bankowości.
Od 1996 roku w bankowości inwestycyjnej. Od 2003 roku w zarządzie OPTOPOL Technology S.A. – jednego z wiodących na świecie producentów urządzeń spektralnej tomografii optycznej, współuczestniczył w rozwoju i wdrożeniu na rynek pierwszego na świecie urządzenia opartego na technologii OCT.
Instytut Chemii Fizycznej Polskiej Akademii Nauk jest wiodącą jednostką badawczą w Polsce. Założony w 1955 roku, może poszczycić się najwyższą kategorią naukową przyznawaną przez Ministerstwo Nauki i Szkolnictwa Wyższego (A+). Instytut ma prawo posługiwać się logo „HR Excellence in Research” co potwierdza dbałość o najwyższe standardy w rekrutacji naukowców, wsparcie w rozwoju ich kariery a także zaangażowanie społeczne pracowników.

Uzyskał Doktorat na Heriot-Watt University w Edynburgu, Wielkiej Brytanii, specjalizuje się w fizyce ultraszybkich laserów Doświadczenie przemysłowe w zakresie BR&I oraz rozwóju systemów laserowych (8 lat MSquared UK), rozwijanie produktów i relacje z klientami, a także proces przygotowywania wniosków patentowych, projektowanie i organizacja laboratorium laserowego oraz zakładu produkcyjnego high-tech, rozwój biznesu high-tech.
profesor Polskiej Akademii Nauk, doktor habilitowany z zakresu zachowania fazowego i dynamiki w roztworach polimerów. Wieloletni pracownik Instytutu Chemii Fizycznej, obecnie pełniący funkcję z-cy dyrektora.
Lekarz, jako pierwszy w Polsce wprowadził model lekarza rodzinnego, Założyciel i współtwórca Grupy Nowy Szpital – największej prywatnej sieci szpitali w Polsce. Uczestniczył i jej rozwoju a następnie sprzedaży funduszowi PENTA Investments.
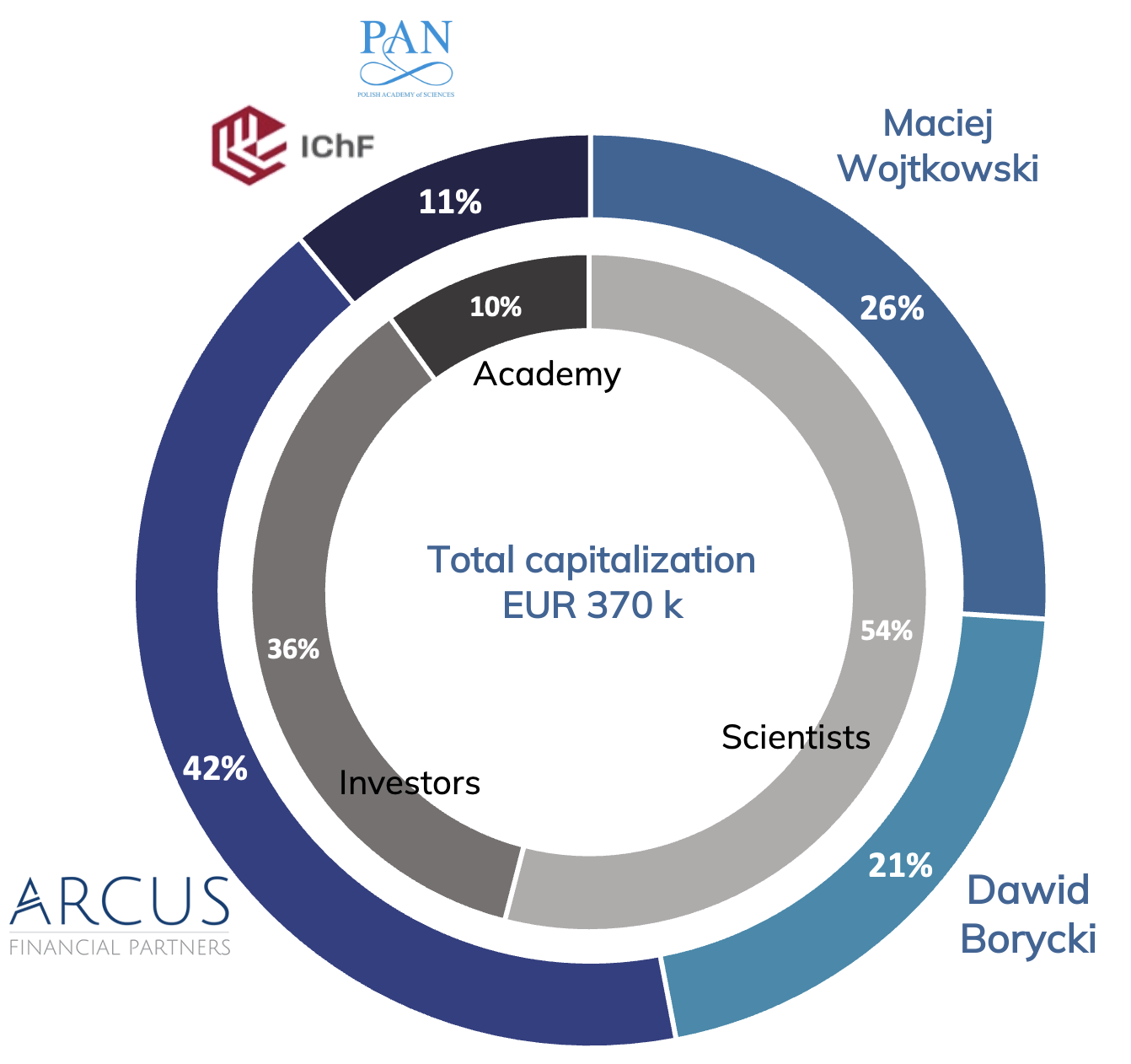
Spółka posiada kapitał zakładowy w 2.2 mln PLN.
Zespół naukowy (twórcy) wraz z Instytutem Chemii Fizycznej PAN posiadają większość udziałów. Pozostałe udziały należą do Arcus Financial Partners